做了大半輩子的新藥研發與測試,臺灣大學心理學系賴文崧教授最常被問的,就是唸心理學的怎麼跑去「賣藥」?他笑著說:「心理學起源於什麼?有人回答是『哲學』,這只答對了一半。心理學的母親是多數人熟知的哲學,而它的父親則是『生理學』。」
一般大眾對心理學的認識較偏向「臨床心理學」,也就是透過心理學理論、量表與心理治療,為心理患者診療。但賴文崧提醒:「心理學其實橫跨了社會科學與自然科學。心理學是研究『心智活動』的科學,除了關注心理狀態,其背後的神經生理機制當然也包含其中,乃至於研究藥物如何影響心智功能的『神經心理藥物學』。」
 自大學起,賴文崧便對「精神疾病」感興趣,為什麼人們會受精神異常所苦?「我想透過研究『不正常』了解解什麼是『正常』?」
自大學起,賴文崧便對「精神疾病」感興趣,為什麼人們會受精神異常所苦?「我想透過研究『不正常』了解解什麼是『正常』?」
拍攝/古佳立
沉默的精神疾病:思覺失調症
若罹患心理疾患,應該要看「精神科」、「神經科」、「身心科」?還是要找「臨床心理師」?對於精神疾病,一般人常以為是心理問題造成,但其實精神疾病的成因複雜且非單一原因造成。如遺傳、腦部受傷、腦內某種神經傳導物質失衡、藥物濫用、環境壓力及心理因素等,都可能影響發病過程與症狀。
以「思覺失調症」(schizophrenia)為例。從心理學的角度來說,賴文崧認為思覺失調症的成因涵蓋了「先天」、「後天」、「先天後天交互作用」、以及「時間(身心發展)」等心理學所關注的重點,非常值得研究。「唸心理學的人很喜歡探討先天與後天的影響。像是你的個性天生如此,抑或後天父母管教太嚴而造成的?但如前面說過,心理問題的背後有神經機制在運作。」
思覺失調症可概分為三大症狀:一是正常人不會出現的「正性症狀」,如幻聽、妄想,甚至有些人會說自己聽到神明的聲音等。二是正常人會有的感受或行為功能但病人缺乏的「負性症狀」,如面無表情、沒有情緒、社會退縮等。三是「認知功能異常」,指的是記憶、執行力與思考等受到影響,致使患者表達困難、執行功能不佳,難以與外界溝通或建立連結。
 近年,「思覺失調」一詞頻繁出現在公眾視線,從震驚全臺的內湖隨機殺人事件(小燈泡)、臺鐵嘉義車站刺警命案,再到話題電視劇《我們與惡的距離》,都與思覺失調症有關。
近年,「思覺失調」一詞頻繁出現在公眾視線,從震驚全臺的內湖隨機殺人事件(小燈泡)、臺鐵嘉義車站刺警命案,再到話題電視劇《我們與惡的距離》,都與思覺失調症有關。
圖片來源/Unsplash
賴文崧指出:「細想一下,這些負性與認知症狀其實都不易被外人察覺,就連病人本身也缺乏病識感。舉個例子,對於家中青春期的孩子,無緣由地情緒不穩、社交退縮,父母往往認為他只是比較宅、不愛跟人互動而已,卻忽略了這可能是好發於青春期晚期或成年期早期的思覺失調症的前驅期。」
「有一部經典電影《美麗境界》(A Beautiful Mind),便是改編患有思覺失調症的諾貝爾經濟學獎得主納許(John Nash, 1928-2015)的人生經歷。我們可以發現,患病的人不僅對幻覺的真實性毫不懷疑,甚至旁人也未必能覺察對方有問題。直到幻覺與妄想嚴重影響生活,比如被迫害妄想及傷害自我或他人,大家才會注意到他們的異常。」
思覺失調症在全世界的盛行率約為百分之一。儘管我們已掌握了相關臨床病徵,但對於思覺失調症的成因與治療(特別是負性與認知症狀),醫療上能做的仍十分有限。賴文崧感概:「看著病人,我們能夠描述他們的病症、做量表評估,但沒有有效的解方。醫生明知病人的痛苦卻無法給予藥到病除的治療,多麼無力!」
想研發新藥?在疾病中找答案
「想要研發新藥,首先要找出思覺失調症的可能致病原因。」
病理上,「NMDA受體」功能低下(NMDA receptor hypofunction hypothesis of schizophrenia)被認為是思覺失調症的可能病因之一。NMDA受體是中樞神經興奮性傳導物質麩胺酸(glutamate)的受體,廣泛分布在中樞神經系統。它參與了許多大腦功能也扮演了重要的調控角色,負責神經訊號的傳送,促進我們的記憶與學習,維持身體協調、情緒與認知功能等。
因此,當腦中特定腦區的NMDA受體功能受損時,便會造成神經系統興奮與抑制失衡或功能低下,導致一些腦區相對應的神經活動及神經傳導過度亢奮或功能低落。患者會出現情緒異常、動作怪異,甚至幻覺、妄想等類似中邪的情況。而這些都是思覺失調的相關症狀。
賴文崧補充道:「之所以會知道NMDA受體是關鍵因素之一,不僅是在遺傳與病理等相關研究中,證實思覺失調症患者死後大腦細胞組織與正常人在NMDA受體相關基因與蛋白質表現上有所差異。同時透過反面驗證,吸食K他命(ketamine)與天使塵(phencyclidine)這類毒品,也會讓人產生類似思覺失調症的情況。原因便是這些毒品有阻斷NMDA受體功能的作用,吸食者會有陷入幻覺、癲狂的行為表現。」
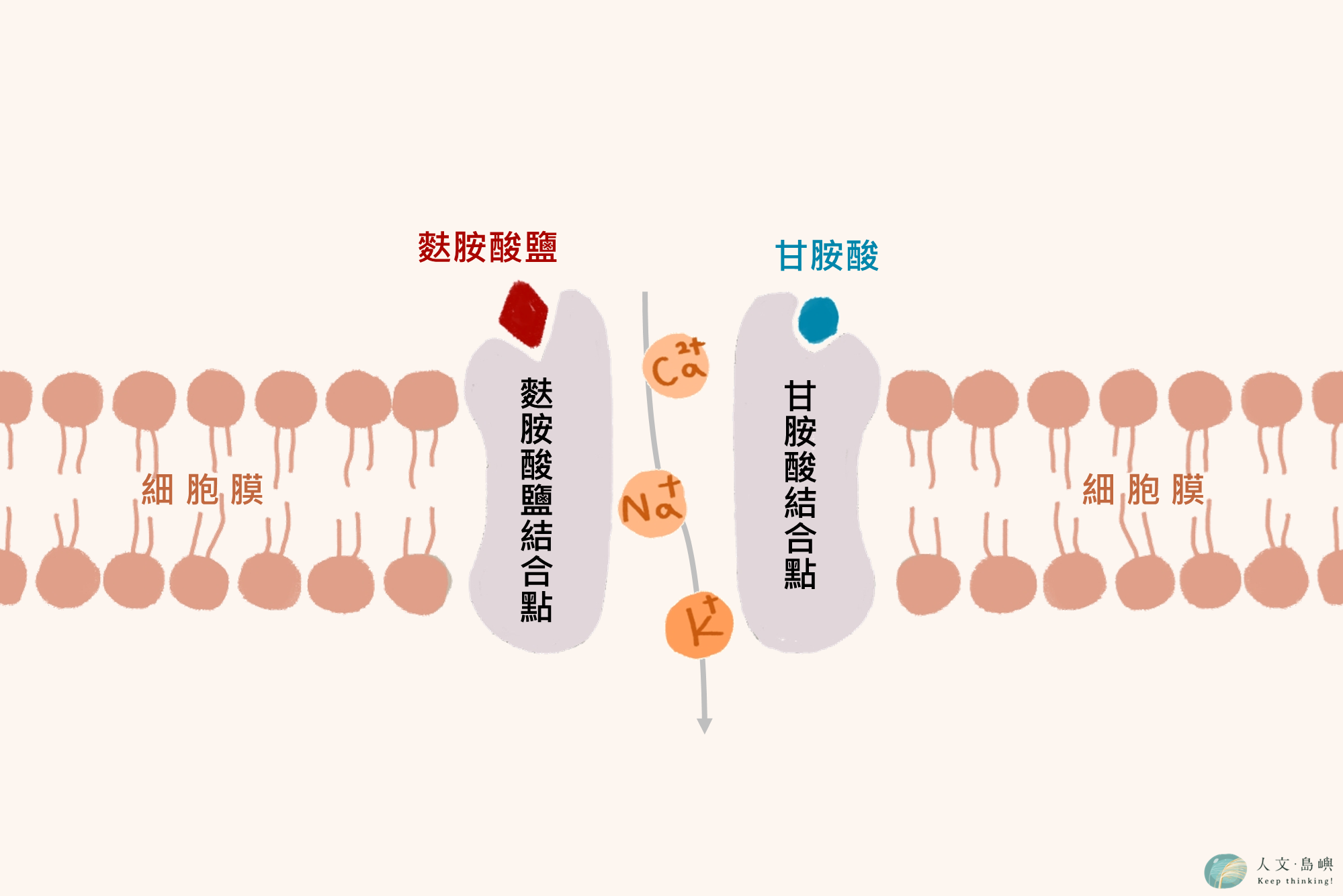 NMDA受體猶如一個甜甜圈般的中空離子通道(ion channel),透過與配體麩胺酸(glutamate)與甘胺酸(glycine)的結合,開啟或關閉離子通道,讓神經細胞間的鈉離子(Na⁺)、鈣離子(Ca2⁺)與鉀離子(K⁺)能進出神經細胞,維持及引發後續神經細胞放電與傳遞神經訊號。
NMDA受體猶如一個甜甜圈般的中空離子通道(ion channel),透過與配體麩胺酸(glutamate)與甘胺酸(glycine)的結合,開啟或關閉離子通道,讓神經細胞間的鈉離子(Na⁺)、鈣離子(Ca2⁺)與鉀離子(K⁺)能進出神經細胞,維持及引發後續神經細胞放電與傳遞神經訊號。
繪者/陳燕琳
然而,儘管知道了強化NMDA受體功能是改善思覺失調相關症狀的途徑之一,但目前仍缺乏安全又有效的藥物。若是正性症狀,市面上的抗精神疾病藥物(antipsychotics)雖或多或少有一些副作用,卻仍有一定程度的改善效果。但對於治療負性症狀與認知功能障礙,迄今仍是『未被滿足的醫療需求』(unmet medical needs)。」
那麼,該如何著手新藥研發?賴文崧說道:「過去沒有直接治療思覺失調症的藥物,在臨床上主要針對病人的某些症狀,醫生會給予抗精神疾病藥物來減輕特定病症。因此我們在2013年組成一個跨領域的研發團隊,經由臨床觀察、臨床前實驗及結合AI大數據比對,改良傳統藥物的缺點,研發小分子化合物並合成一系列能促進NMDA受體功能的胺基酸氧化酶 (D-amino acid oxidase, DAO)抑制劑。」
「經過多年反覆的試驗與檢測,其中編號RS-D7的新藥在細胞試驗及小鼠動物試驗中,皆可以有效提升NMDA受體功能並改善動物思覺失調症相關行為。研發過程中也發現一個上市多年但並非用於治療中樞神經系統的藥物RS-D7pro,其中代謝物之一恰巧與RS-D7的成分相同。」
「所以我們進一步與臺大醫院精神科合作,先給予病患八週的RS-D7pro,他們在四週內症狀顯著改善。初步試驗證實此藥物能有效緩解病患的負性症狀與認知功能失調,值得進行後續正式臨床試驗以驗證RS-D7的功效。」
一款藥治兩種病?
在確認了NMDA受體功能異常是導致人們產生許多不正常行為的一大原因後,賴文崧與團隊透過文獻回顧以及研發團隊的研究數據,進一步發現RS-D7可能有其他精神/神經疾病的適應症,能治療其他因NMDA受體功能異常而引發的病症。
接續,他們透過動物實驗,證實RS-D7具有的提升NMDA受體功能以及改善腦中發炎反應的功效,很有機會適用於治療其他中樞神經系統疾病。像是阿茲海默症(Alzheimer’s disease)、妥瑞氏症(Tourette syndrome)、輕度認知功能障礙(mild cognitive impairment)與多重系統退化症(multiple system atrophy)等。
據此,賴文崧與團隊從2017年起便進一步針對「多重系統退化症」展開藥效測試。它是一種罕見但惡化快速且致命的神經退化性疾病。患者會產生動作緩慢、平衡失調、小腦萎縮、認知功能退化、及自主神經系統失調等症狀。發病時通常會出現兩個以上的神經系統退化症狀,約80%的患者在發病後五年內會變得失能,從發病到死亡的時間平均是八年。
 有許多精神疾病與生理疾病的病因,其實都與腦部神經系統功能異常有關。
有許多精神疾病與生理疾病的病因,其實都與腦部神經系統功能異常有關。
圖片來源/Unsplash
「與其說我們特別鎖定多重系統退化症,不如說是這個疾病的病患與家屬找上我們。因為相較於其他病症,該病症目前仍無藥可醫。在全世界的盛行率約為十萬分之五,許多國家都將它列為罕病。但在臺灣尚未新增為罕見疾病,病人也就無法得到更多健保上的幫助,一般人的關注度自然也不高。種種現實因素,都降低了藥商為該疾病進行藥物研發的意願。」
因此,近期正在進行中的RS-D7人體臨床試驗,賴文崧與團隊也優先選擇以治療多重系統退化症為首要目標。他解釋:「不僅是因為多重系統退化症的病人病逝太快,在臺灣是很弱勢的群體,還考量到在進行藥物試驗的過程中,會需要相當數量的臨床病人。而多重系統退化症主要反映於病人的動作功能上,例如走路有沒有問題,相對容易量測出來,診斷與評估上相對客觀,較無模糊空間。這些都有利於新藥的研發與臨床試驗。」
反觀思覺失調症這類精神疾病診斷上則相對主觀和困難,治療上也容易有「安慰劑效應」(placebo effect)現象。意思是醫生進行問診及開藥的行為本身就有可能讓病人感覺好轉的功效,但事實未必如此。再者,也常發生問診與治療時病人每次自我陳述內容隨著病況出現不一致的情況,致使診斷不易精確,難迅速客觀做出藥效評估。
「為了讓這項救命之藥能及早送到病人手中,我們選擇先主攻多重系統退化症。經過多年努力,我們先後在動物與病患的初步臨床試驗中都得到令人期待的實驗結果。RS-D7也於2022年順利取得美國食品藥物管理局的『孤兒藥資格」(意即罕見疾病用藥)。」
「接續進行中的多重系統退化症人體臨床試驗,我們也會視情況著手針對思覺失調症,申請臨床試驗許可與推動臨床試驗。而且,奠基於進行中的臨床一期安全性測試結果,之後針對思覺失調症的檢驗過程,應該可以走得更快更穩健!」
 賴文崧與團隊以「治療多重系統退化症的新希望」分別榮獲2022年未來科技獎(亮點技術)以及2023年國家新創獎(學研新創)。今年(2024年)預計將開始在臺灣針對多重系統退化症病患進行新藥的臨床一期與二期試驗,提早實現我們盡快給臺灣病患使用到藥物的承諾。期盼能真正帶給病患及家屬治療的新希望。
賴文崧與團隊以「治療多重系統退化症的新希望」分別榮獲2022年未來科技獎(亮點技術)以及2023年國家新創獎(學研新創)。今年(2024年)預計將開始在臺灣針對多重系統退化症病患進行新藥的臨床一期與二期試驗,提早實現我們盡快給臺灣病患使用到藥物的承諾。期盼能真正帶給病患及家屬治療的新希望。
圖片提供/賴文崧
「此次採訪,講述新藥研發的歷程不到兩個小時。但這條路,整個團隊篳路藍縷走了十年才走到這裡,可謂「十年磨『兩件』。」所以除了感謝團隊同仁與學生們的辛勞外,賴文崧想以自身經驗,鼓勵心理相關科系的師生勇於進行跨領域的研究與合作,走入實驗室與醫院,接觸病人及家屬,看見他們在心理及生理上的痛苦與需求,努力嘗試釐清作用機制並找出解方。
「新藥研發是艱難且極具挑戰性的。但……有機會為患者和我們的社會帶來改變,這一切都是值得的。」(Drug development is hard and very challenging. But… the opportunity to make a difference for patients and our society makes it all worthwhile.)
採訪撰稿/徐瑜棉
攝影/古佳立
編輯/馬藤萍
研究來源
賴文崧(2023)。跨領域建構治療多重系統退化症的新希望:從NMDA受體調控藥物、臨床前模式到臨床試驗。國科會專題研究計畫 (一般策略專案計畫)。
賴文崧(2019)。以NMDA受體功能不足小鼠模式探討一個新穎D-胺基酸氧化酶抑制劑調節思覺失調症相關缺損之功效以及相關神經機制。國科會專題研究計畫(一般研究計畫)。
賴文崧(2013)。從生物心理學取向以Akt1基因缺損小鼠為模式探討先天易染基因與基因-環境交互作用對於與精神分裂症相關之認知功能缺損的行為神經改變與藥物篩選。國科會專題研究計畫(優秀年輕學者研究計畫)。
參考資料
羅達中、賴文崧(2023)。治療多重系統退化症的新希望。人文與社會科學簡訊,第24卷2期,頁69-74。
賴文崧(2020)。您所不知道的心理學?開拓心智研究及精神疾病藥物研發的美麗「心」世界。臺大校友雙月刊,第129期,頁44-48。
賴文崧、羅達中(2020)。為絕症尋找「仙丹」─共濟失調症新藥研發與篩檢測試平台。人文與社會科學簡訊,第21卷2期,頁16-23。
Luo, D. Z., Chang, C. Y., Huang, T. R., Studer, V., Wang, T. W., & Lai, W. S. (2020). Lithium for schizophrenia: supporting evidence from a 12-year, nationwide health insurance database and from Akt1-deficient mouse and cellular models. Scientific Reports, 10(1), 647.
Pei, J. C., Hung, W. L., Lin, B. X., Shih, M. H., Lu, L. Y., Luo, D. Z., Tai, H. C., Studer, V., Min, M. Y., & Lai, W. S. (2019). Therapeutic potential and underlying mechanism of sarcosine (N-methylglycine) in N-methyl-D-aspartate (NMDA) receptor hypofunction models of schizophrenia. Journal of Psychopharmacology, 33(10), 1288-1302.

 本著作由人文·島嶼著作,以創用CC 姓名標示–非商業性–禁止改作 4.0 國際 授權條款釋出。
本著作由人文·島嶼著作,以創用CC 姓名標示–非商業性–禁止改作 4.0 國際 授權條款釋出。